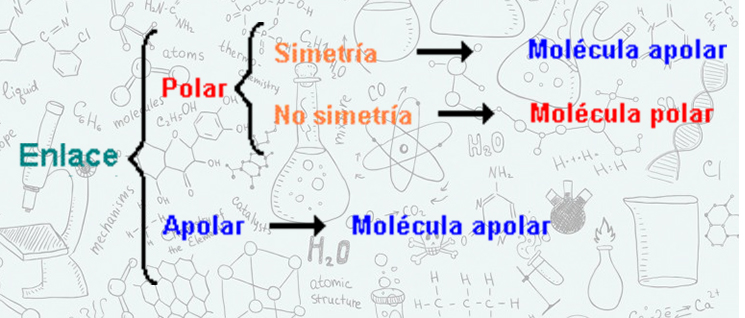
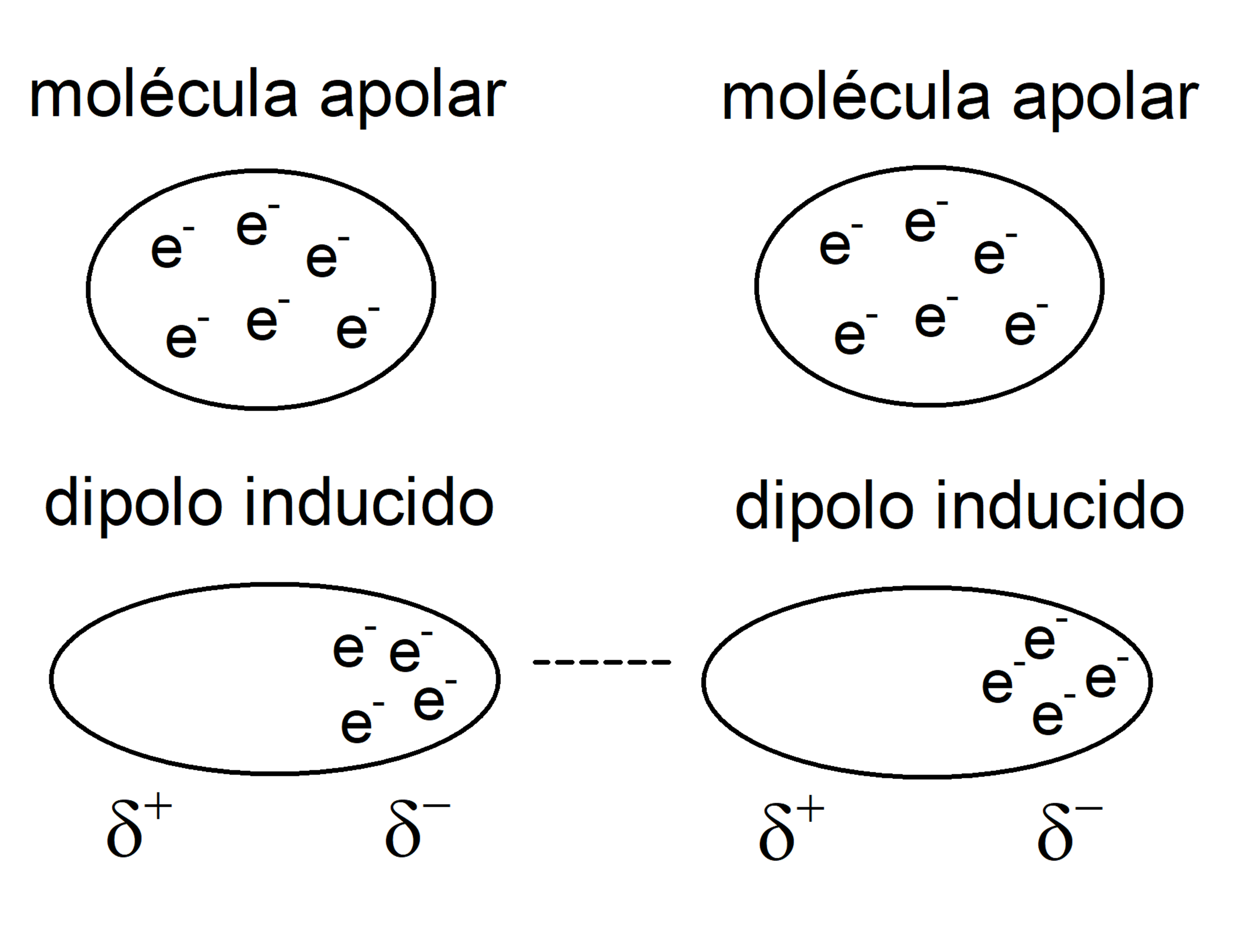El Agua es una Molécula Polar | Capítulo 5: La Molécula de Agua y la Disolución | Middle School Chemistry

Solubilidad Cuantitativamente, concentración de soluto en solución saturada a determinada temperatura Cualitativamente, interacción espontánea entre soluto. - ppt video online descargar

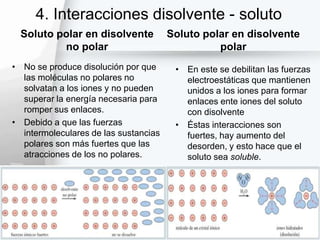
Las fuerzas intermoleculares controlan algunas de las propiedades de las sustancias moleculares, por ejemplo, el punto de ebullición y la solubilidad
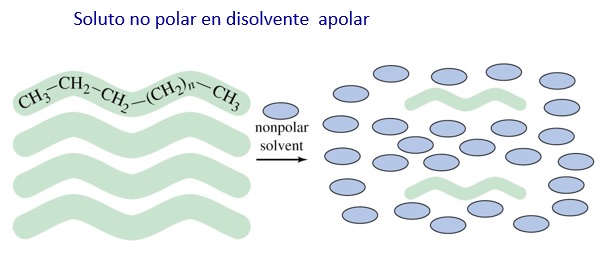
Las fuerzas intermoleculares controlan algunas de las propiedades de las sustancias moleculares, por ejemplo, el punto de ebullición y la solubilidad

Las fuerzas intermoleculares controlan algunas de las propiedades de las sustancias moleculares, por ejemplo, el punto de ebullición y la solubilidad